Fuentes de datos y metodología
Cómo recopilamos, clasificamos y actualizamos la evidencia médica en la que se basa Evidence AI.
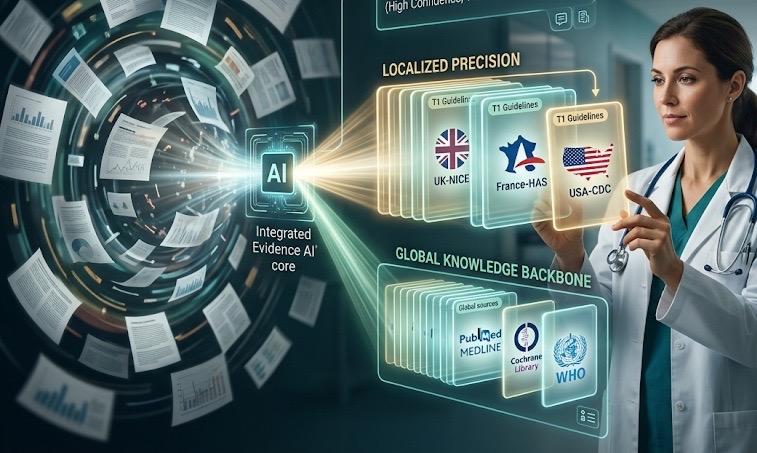
ElfieCare Evidence AI se basa en un sistema de conocimientos médicos seleccionado y regulado, y no en un motor de búsqueda de uso general. Cada respuesta se fundamenta en fuentes externas verificables, se clasifica según el nivel de solidez de la evidencia y se mantiene actualizada mediante revisiones estructuradas.
En esta página se explica cómo funciona.
Nuestros principios
- Solo verdad externa. Todo el conocimiento procede de fuentes externas verificables. El sistema no genera datos médicos.
- La gestión antes que el uso. No se muestra nada a los médicos hasta que no se haya estructurado, clasificado y revisado.
- La honestidad por encima de la cobertura. Cuando las pruebas brillan por su ausencia, son débiles o contradictorias, el sistema está diseñado para decirlo así, con claridad y sin especulaciones.
- Trazabilidad. El sistema está diseñado para registrar la base empírica, el nivel de confianza y el proceso de resolución de cada respuesta, lo que facilita las auditorías y la gobernanza clínica.
1. Qué indexamos
Evidence AI se basa en un registro seleccionado de fuentes médicas, organizado en tres niveles.
1.1 Base de datos mundial de pruebas
Estas fuentes universales sirven de base para cualquier consulta clínica, independientemente de la ubicación del médico.
1.1.1 Publicaciones de acceso abierto y registros de ensayos clínicos
- PubMed / MEDLINE: el mayor índice de literatura biomédica del mundo, que ofrece resúmenes estructurados de todas las revistas indexadas.
- PubMed Central (PMC): millones de artículos de investigación de acceso abierto en texto completo.
- ClinicalTrials.gov y la Plataforma Internacional de Registros de Ensayos Clínicos (ICTRP) de la OMS: datos de ensayos en curso y finalizados para mantener la actualidad clínica.
- Biblioteca Cochrane: resúmenes estructurados y resúmenes en lenguaje sencillo de la referencia por excelencia en revisiones sistemáticas.
1.1.2 Autoridades sanitarias mundiales
- Organización Mundial de la Salud (OMS): directrices, datos sobre la carga de morbilidad y calendarios de vacunación.
- Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU.: recomendaciones de salud pública y calendarios de vacunación.
- Institutos Nacionales de Salud (NIH): resúmenes de investigaciones y orientaciones clínicas.
- Administración de Alimentos y Medicamentos de los Estados Unidos (FDA): prospectos de medicamentos, comunicaciones sobre seguridad y advertencias de recuadro negro.
- Agencia Europea de Medicamentos (EMA): información sobre la seguridad y la autorización de medicamentos en Europa.
1.1.3 Revistas de acceso abierto revisadas por pares
JAMA Network Open, Journal of Medical Internet Research (JMIR), BMC Medicine, PLOS Medicine, Frontiers in Medicine, Diabetes Care y otras publicaciones que se difunden bajo licencias abiertas sin restricciones comerciales.
En el caso de las revistas más prestigiosas, cuyo acceso al texto completo requiere una licencia, indexamos los resúmenes estructurados disponibles a través de PubMed. Estos incluyen los resultados clave, el diseño del estudio, los tamaños del efecto y las conclusiones clínicas. Cada entrada basada en un resumen se identifica de forma clara para que el sistema pueda indicar esta limitación.
1.2 Directrices internacionales especializadas
Evidence AI recopila las guías de práctica clínica de las principales asociaciones médicas internacionales y organismos especializados, siempre que dichas guías estén disponibles de forma abierta.
- Asociación Americana de Diabetes (ADA) — Normas de atención médica, publicadas anualmente en acceso abierto.
- Sociedad Americana de Enfermedades Infecciosas (IDSA): guías de práctica clínica.
- KDIGO (nefrología), GINA (asma), GOLD (EPOC), mhGAP de la OMS (salud mental), Organización Mundial de Gastroenterología (WGO): guías especializadas de referencia mundial publicadas en acceso abierto.
- Federación Internacional de Ginecología y Obstetricia (FIGO), Colegio Americano de Médicos (ACP), Federación Mundial de Sociedades de Anestesiólogos (WFSA).
Algunas directrices de sociedades especializadas exigen la firma de acuerdos de licencia comercial. Cuando aún no se hayan formalizado dichos acuerdos, el sistema no incorpora el contenido. Cuando las publicaciones conjuntas o los informes de consenso estén disponibles a través de canales de acceso abierto, se incluyen esos elementos concretos.
1.3 Fuentes normativas y directrices locales
Evidence AI tiene en cuenta la ubicación geográfica. Utiliza el país y la especialidad del médico para dar prioridad a las fuentes normativas y de directrices locales frente a las internacionales.
Recopilamos información de las autoridades sanitarias nacionales, los organismos reguladores de medicamentos y los organismos locales encargados de elaborar guías clínicas en todos nuestros mercados de lanzamiento, entre los que se incluyen:
- Reino Unido — Directrices del NICE, vías clínicas del NHS, datos sobre la seguridad de los medicamentos de la MHRA.
- Francia — Alta Autoridad Sanitaria (HAS), ANSM, Ministerio de Sanidad.
- Australia — Ministerio de Sanidad y Atención a las Personas Mayores, TGA, PBS, Sociedad Australiana de Diabetes.
- Estados Unidos — CDC, FDA, NIH, USPSTF.
- Brasil — Ministerio de Salud, ANVISA, CONITEC, Sociedad Brasileña de Cardiología (SBC).
- España — AEMPS, guiasalud.es, SEOM.
Otras fuentes locales cubren mercados de toda América Latina, Oriente Medio y el norte de África, el África subsahariana y el sudeste asiático. La lista completa de fuentes locales se gestiona internamente y se amplía a medida que se incorporan nuevos mercados.
2. Lo que no indexamos
Somos transparentes en cuanto a nuestros límites.
2.1 Contenido con licencia
Varias guías médicas importantes y bases de datos de referencia están protegidas por derechos de autor o condiciones de licencia que restringen su uso comercial. Respetamos estas restricciones. Cuando no existen acuerdos de licencia, no se incorpora el contenido, independientemente de su valor clínico.
Estamos buscando activamente colaboraciones para ampliar nuestra cobertura allí donde las licencias lo permitan.
2.2 Contenido que no cumple con los estándares de calidad
El sistema no indexa:
- Contenido no revisado por pares, como entradas de blog, comentarios en redes sociales o artículos de opinión sin evaluación de la evidencia.
- Preimpresiones que no han sido sometidas a revisión por pares.
- Materiales de marketing, independientemente de su origen.
- Protocolos internos del hospital que no se han compartido ni validado explícitamente a través de nuestra función de directrices a nivel de espacio de trabajo.
Todas las fuentes que se incorporan al sistema deben superar un proceso de calificación de fuentes en el que se comprueba su legitimidad, su categoría de autoridad, el tipo de documento y la actualidad de la publicación antes de que comience la extracción.
3. Cómo establecemos la jerarquía de la evidencia
No todas las pruebas tienen el mismo peso. Un metaanálisis de varios ensayos controlados aleatorios tiene más peso que un único informe de caso. Para un médico de un país determinado, una guía específica de ese país tiene prioridad sobre una recomendación global. Evidence AI codifica estas distinciones de forma estructural.
3.1 Niveles de evidencia
Cada elemento de conocimiento se clasifica en uno de los cinco niveles de evidencia:
Nivel | Tipo | Ejemplos
T1 | Guías clínicas: adaptadas a la región o de ámbito mundial | Guías de las autoridades nacionales, recomendaciones de la OMS
T2 | Revisiones sistemáticas y metaanálisis | Revisiones Cochrane, síntesis de evidencia de alta calidad
T3 | Ensayos primarios | Ensayos controlados aleatorios
T4 | Evidencia observacional | Estudios de cohortes, estudios de casos y controles
T5 | Consenso y evidencia de nivel inferior | Opinión de expertos, series de casos, declaraciones de consenso
3.2 Marco GRADE
Cuando procede, los elementos de evidencia se caracterizan con mayor detalle mediante el marco GRADE (Grading of Recommendations, Assessment, Development, and Evaluations), que recoge el grado de certeza de la evidencia, la solidez de la recomendación y aspectos de calidad específicos, como el riesgo de sesgo, la inconsistencia, la indirecta y la imprecisión.
3.3 Normas de resolución
Cuando una consulta devuelve resultados procedentes de varias fuentes, el sistema aplica reglas de resolución estructuradas:
- Lo local prima sobre lo global: para un médico de ese país, las directrices locales tienen prioridad sobre las globales.
- Lo más reciente antes que lo antiguo: cuando las fuentes tienen el mismo nivel de evidencia, se da preferencia a las recomendaciones más recientes.
- Nivel de evidencia superior frente a inferior: por categoría y nivel de evidencia.
- Se mantiene el desacuerdo: cuando no es posible resolver un conflicto entre fuentes fiables, se presentan ambos puntos de vista con las referencias completas. El sistema está diseñado para poner de manifiesto el desacuerdo, en lugar de ocultarlo sin decir nada.
3.4 Puntuación de confianza
Cada objeto de conocimiento lleva asociada una puntuación de confianza compuesta que se deriva de dos componentes:
- Calidad: nivel de evidencia, clasificación GRADE, exhaustividad de la gobernanza y existencia de conflictos de intereses.
- Actualidad: antigüedad de la fuente en relación con la periodicidad de las revisiones, la reciente actualización, el estado del ciclo de vida y si la organización de origen ha publicado alguna actualización.
Esta puntuación determina el comportamiento de recuperación:
- Alto nivel de confianza — citado con seguridad. Formulación: «Las pruebas respaldan…»
- Confianza moderada — se cita con reservas explícitas. Formulación: «Las pruebas sugieren que…»
- Baja fiabilidad: se menciona únicamente cuando no se dispone de pruebas más sólidas. Formulación: «Las pruebas limitadas indican que…»
- Confianza insuficiente: excluido de los resultados clínicos y en cola para su revisión.
Cuando las pruebas son insuficientes o inexistentes, el sistema está diseñado para indicarlo explícitamente y ofrecer opciones para refinar la consulta de forma estructurada, en lugar de generar una respuesta especulativa.
4. Cómo nos mantenemos al día
La evidencia médica tiene una vida útil limitada. Las guías clínicas se actualizan, se publican nuevas alertas de seguridad y los tratamientos que antes eran estándar quedan obsoletos. Una base de conocimientos estática se deteriora silenciosamente. Evidence AI aborda este problema mediante cinco mecanismos interrelacionados.
4.1 Cadencia de revisión
A cada elemento de conocimiento se le asigna una periodicidad de revisión en función del riesgo clínico y la volatilidad prevista:
Clase | Frecuencia | Alcance
A | 3-6 meses | Evidencia de alto riesgo y en rápida evolución: directrices terapéuticas, alertas sobre la seguridad de los medicamentos
B | 6-12 meses | Directrices clínicas fundamentales y afecciones comunes
C | 12–24 meses | Conocimientos básicos sólidos
D | Bajo demanda | Contenido de baja prioridad o histórico
4.2 Revisiones activadas por eventos
La cadencia programada se complementa con desencadenantes de revisión basados en eventos:
- Una organización de referencia publica una nueva versión de la guía.
- Una autoridad reguladora de medicamentos publica una actualización sobre seguridad.
- Están surgiendo datos contradictorios de alto nivel.
- El sistema detecta una contradicción entre los objetos de conocimiento existentes.
- Se identifica una retractación de una fuente o una fe de erratas publicada, lo que desencadena una reacción en cadena inmediata en el ciclo de vida.
4.3 Pérdida de frescura
El componente de actualidad de la puntuación de fiabilidad de cada objeto se va reduciendo con el tiempo, en función de la periodicidad de su revisión. Las pruebas que evolucionan rápidamente (Clase A) pierden vigencia más rápidamente que los conocimientos estables (Clase C/D). Si la fiabilidad de un objeto cae por debajo de un umbral de seguridad, el sistema está diseñado para marcarlo automáticamente para su revisión y restringir su uso en los resultados clínicos.
4.4 Etapas del ciclo de vida
Cada objeto de conocimiento se encuentra en uno de estos cuatro estados:
- Activo: vigente, válido, susceptible de ser recuperado.
- Precaución: se puede utilizar, pero está marcado debido a su antigüedad, a un conflicto parcial o a que está pendiente de revisión.
- Obsoleto: sustituido por pruebas más sólidas o recientes, o fuente retirada.
- Retirado: fuera de servicio, conservado para fines de auditoría.
4.5 Revisión clínica y detección de contradicciones
Los objetos de evidencia son gestionados por revisores clínicos cualificados. Los objetos de alto riesgo se someten a una doble revisión. Las discrepancias entre los revisores se remiten a un nivel superior y deben resolverse antes de que se apruebe el uso de un objeto. Las revisiones se registran para garantizar la trazabilidad.
El sistema también supervisa si existen conflictos entre los objetos de conocimiento. Cuando una nueva directriz contradice a una ya existente, se señala la contradicción y se remite para su revisión. En la interfaz destinada al médico, los conflictos no resueltos se presentan incluyendo ambos puntos de vista y las referencias bibliográficas; el sistema está diseñado para que sea el médico quien tome la decisión.
Solo para uso profesional. ElfieCare Evidence AI sintetiza la literatura médica basándose en parámetros clínicos. No ofrece diagnósticos médicos ni prescribes tratamientos. La decisión clínica final corresponde al profesional sanitario.




